化学方程式的配平很重要,考试中会考化学方程式的书写以及相关计算,如果化学方程式书写就错了,那后面的计算就白出力了。
化学方程式的配平有多种方法,在这只讲三种常用方法,在初中学习阶段,这三种方法已足够。
一、观察法
初中许多化学方程式比较简单,通过简单的观察就能配平。
方法:从化学式较复杂的物质入手,根据质量守恒定律,推求反应物和生成物的化学计量数,直至配平。
步骤:(1)从化学式较复杂的一种生成物推求有关反应物化学式的化学计量数和这一生成物的化学计量数;
(2)根据求得的化学式的化学计量数,再找出其它化学式的化学计量数,这样即可配平。
例如:Fe2O3 + CO——Fe + CO2
观察:
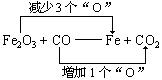
所以,1个Fe2O3应将3个“O”分别给3个CO,使其转变为3个CO2。
即Fe2O3 + 3CO——Fe + 3CO2
再观察上式:左边有2个Fe(Fe2O3),所以右边Fe的系数应为2。
即Fe2O3 + 3CO -----2Fe + 3CO2
这样就得到配平的化学方程式了,注意将“—”线变成“=”号。
即Fe2O3 + 3CO == 2Fe + 3CO2
【练习】
1、 CO + Fe3O4 —— Fe + CO2
2、 C + Fe2O3—— Fe + CO2
二、最小公倍数法
方法: 找出式子两边只出现一次,并且原子数相差较大的元素,求出最小公倍数,进而确定反应物和生成物的化学计量数。
步骤:(1)求出每一种原子在反应前后的最小公倍数;(2)使该原子在反应前后都为所求出的最小公倍数;(3)一般先从氧原子入手,再配平其他原子。
例: 配平Al + Fe3O4 → Fe + Al2O3
第一步:配平氧原子 Al + 3Fe3O4 ---- Fe + 4Al2O3
第二步:配平铁和铝原子 8Al + 3Fe3O4 ---- 9Fe + 4Al2O3
第三步:配平的化学方程式 8Al + 3Fe3O4 -----9Fe + 4Al2O3
【练习】
1、 Al + O2—— Al2O3
2、 Fe + O2—— Fe3O4
三、定一法
适用条件:如大多数碳氢化合物或含碳氢氧的化合物与氧气的反应,以及某些分解反应。
配平:
解析:先设定C2H5OH的系数为1,再确定CO2的系数为2,H2O的系数为3。方程式右边氧原子总数为7,C2H5OH中有一个氧原子,可确定O2的系数为3。
配得结果为
【练习】
1、 C2H2 + O2 —— CO2 + H2O
2、 C6H6 + O2 —— CO2 + H2O



